Gclustを活用してDGDG合成酵素遺伝子を特定。さらに,和田研究室とのコラボレーションで光合成におけるDGDGの役割を解明
1.光合成に大切な糖脂質の合成経路
葉緑体やシアノバクテリアの膜には糖脂質が多く含まれている。特にガラクトースを1個含むMGDGや2個含むDGDGは光合成膜に主に含まれ,生物が作る脂質の中で最も量が多く,光合成には重要だと考えられている。DGDG合成酵素は植物や緑藻ではすでに発見されていて,DGD1と命名されている。さらに連続的にガラクトースを結合していく別の酵素もあると考えられているが,これはまだ発見されていない。ところが,シアノバクテリアや紅藻のゲノムが解析されたときに,植物のDGD1に相当する酵素の遺伝子が見つからないことがわかった。そこで,シアノバクテリアと紅藻でDGDGを合成している酵素を探すため,これらの生物に共通に存在するタンパク質から糖転移酵素モチーフを持つものを見つけようと考えた。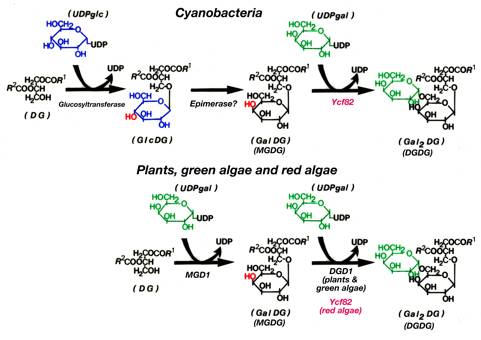
図1:シアノバクテリアと植物や藻類における糖脂質合成経路の比較
Sato and Murata (1982) Biochim. Biophys.
Acta 710: 271-278, 279-289に基づき,最近発見された酵素を加えた。斜体は構造式と区別するためで,遺伝子を表す斜体ではない。また,Ycf82は今回新たに機能解析したもの。
2.Gclustサーバーによる検索
すでに佐藤研究室で開発していたGclustを用いると,このような検索が簡単にできる。GclustサーバーからCZ36wというデータセットを選び,CyanoとCMEをyesに,ATHとGreenをnoに,その他をanyとして,サーチすると,72個の相同タンパク質グループが表示される。ほとんどは光合成に関わるタンパク質が出てくる。これは,紅藻とシアノバクテリアには光を集める色素系としてフィコビリソームがあり,これに関連したタンパク質が皆このパターンになるからである。しかしその他に機能がわからないものもある。Ycf番号が付けられたものは,まだたくさんのゲノムが解読される前に葉緑体ゲノムに共通してコードされるタンパク質や,シアノバクテリアにも共通にコードされているタンパク質に対して番号付けがされたものである。100種類以上の番号がついているが,その中には,すでに光合成に重要な機能を持つことがわかったものも多い。表示されたリストの中で,アノテーションを見ていくとクラスター1816にはprobable glycosyltransferase(「糖転移酵素の可能性がある」という意味)と書かれている。左の番号をクリックして,実際にクラスターに属するタンパク質を見てみると,確かに紅藻とシアノバクテリア全部に共通にあることがわかる。他の生物にも少しあるが,これらの生物にDGDGがあるのかわからない。このように系統プロファイルを使う検索では,遺伝子を持っていると思われる生物の範囲を限定しすぎないことがよいようである。しかも紅藻ではCMEのあとにcがついていて,葉緑体ゲノムにコードされていることがわかり,Ycf82という番号がついていることもわかる。これがDGDG合成に関わる糖転移酵素ではないかとねらいをつけ,遺伝子操作が容易なSynechocystis sp. PCC 6803というシアノバクテリアを使って,対応する遺伝子であるsll1508を破壊したところ,見事にDGDGを含まない変異体が得られたのである。
なお,実際の検索は2年以上前に行ったので,Gclustの古いバージョンで,データセットCZ20x0を使った。GclustサーバーのOld versionsから2006-06を選び,クラスター2825を見ると,上記と同じクラスターにあたることがわかる。
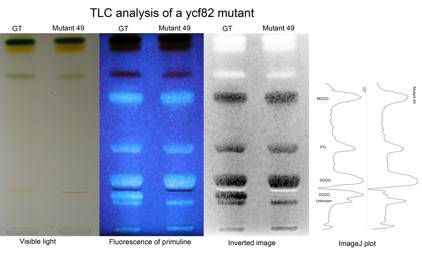
図2:遺伝子破壊株49と親株GTの脂質分析
薄層クロマトグラフィー(TLC)を用いて細胞全体の脂質を展開し(左の写真),プリムリンという蛍光色素による蛍光で脂質を検出した(中央の写真)。上から,MGDG, PG, SQDG, DGDG, 不明物質となる。49株に本当にDGDGがないことを見やすくするため,画像を反転した(右の写真)。同じものをImageJを用いてデンシトグラムでも示した(一番右のグラフ)。同様の結果は,下記の和田研によるタグ付き変異体でも確認された。
3.光合成におけるDGDGの役割
DGDGを作ることができないシアノバクテリアの変異株49は,あまり強くない光のもとでは,野生株と変わらない成長を示した。つまり,DGDGは必須ではないということになる。これはおそらく他の脂質が存在することにより,膜構造が保たれるためと考えられる。しかし,パルス変調蛍光解析の結果,Fvが小さく,わずかな光で光合成電子伝達が飽和してしまうことがわかった。
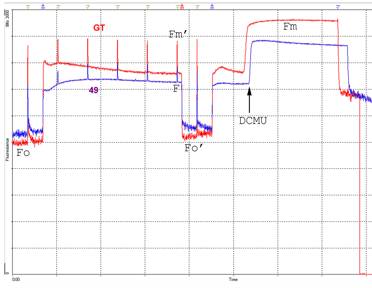
図3:パルス変調(PAM)蛍光解析の一例
この測定法を使うと,測定光は交流変調がかかっているため,出てくる蛍光も変調されている。そのため,蛍光を他の光と分離して検出することができ,光合成に働く光を当てながらでも蛍光測定ができる。測定は左から右に向かって進む。測定光を当て始めてからの蛍光レベル(相対値)を表示している。所々で光合成が飽和するパルス光を当てているため,ピークが描かれている。測定開始後1分後から,光合成作用光をあてているので,蛍光レベルが高くなり,やがて一定に落ち着く。その後,Fのマークのあとで作用光を切り,再び作用光なしでの蛍光レベルを調べる。最後に作用光をあて,光合成の阻害剤であるDCMUを加えることにより,光化学系IIからの最大蛍光レベルを求める。これらの値をもとに光合成を特徴づける指標を計算するが,ここでは省略する。GTと49を比較した場合,作用光を当てているときの定常レベルに比べ,飽和パルス光を当てたときのピークが49では小さいことがわかる。このピークの高さ(Fv)は,光合成電子伝達で電子を流す余裕を表し,これが少ないと,すぐに電子が詰まって流れなくなってしまう。そうすると,余った光エネルギーが散逸できなくなり,光化学系を破壊するなどの傷害が起きることがある。DGDG欠損変異体では,光化学系表在タンパク質がはずれやすくなっていて,そのために電子伝達が十分にできなくなっていると考えられる。
これをさらに詳しく解析するため,和田元(わだ はじめ)先生の研究室と共同研究を行い,変異体の光合成に関する性質を調べた。このために,ヒスチジンタグを持つ光化学系IIのタンパク質を発現する株を用いて,DGDGを作らない変異を導入した。この変異株から光化学系II複合体を精製したところ,酸素発生活性が低く,表在性タンパク質のPsbU, PsbV, PsbOなどがはずれていた。さらに変異体細胞では光合成の熱安定性も低下していた。細胞内でもこれらの表在性タンパク質がはずれやすくなっていることを示していると考えられる。すでに明らかにされている光化学系II複合体の立体構造では脂質分子の存在位置も調べられていて,少なくとも4分子のDGDGが結合していると考えられている。今回の結果は,光化学系II複合体に存在するDGDGが,サブユニットの結合の安定化に働いていることを示している。これらのDGDGはおそらく他の脂質分子によって埋め合わせされているものと想像されるが,ガラクトースを2個もつということが,光化学系II複合体の構造安定化に必要だと考えることができる。
論文
I.
Sakurai, N. Mizusawa, H. Wada and N. Sato (2007) Digalactosyldiacylglycerol
is required for stabilization of the oxygen-evolving complex in photosystem II.
Plant Physiol.
(accepted)
N.
Sato and T. Moriyama (2007) Genomic and biochemical analysis of lipid
biosynthesis in the unicellular rhodophyte Cyanidioschyzon merolae: lack of plastidic desaturation pathway
results in mixed pathway of galactolipid synthesis. Eukaryotic Cell 6: 1006-1017.
(2007年9月27日作成)